Pracownia Wspomagania Diagnostyki i Terapii Układu Krążeniowo-Oddechowego
Zespół
dr inż. Krzysztof Zieliński – Kierownik Pracowni
Prof. dr hab. inż. Marek Darowski
Dr hab. inż. Tomasz Gólczewski, profesor IBIB PAN
Dr inż. Maciej Kozarski
Dr n. med. Jeremi Mizerski
Dr inż. Krzysztof Pałko
Dr inż. Barbara Stankiewicz
Dr inż. Anna M Stecka
Obecna tematyka badawcza
A. Symulatory i modele komputerowe
Proponowanie nowej lub ulepszonej aparatury i nowych lub ulepszonych metod wspomagania i testowania układu krążenia i oddechowego jest tematem wiodącym w Pracowni od momentu jej powstania. Ponieważ wstępne testowanie nowych rozwiązań na żywych pacjentach nie wchodzi w grę z powodów etycznych, rozwijaliśmy metody symulacyjne. Na szczególną uwagę zasługuje zbudowanie sztucznego pacjenta oddechowo-krążeniowego (Kozarski et al., 2015; Zieliński et al., 2019a; Zieliński et al., 2019b, Fresiello et al., 2020; Zieliński et al., 2020; Zieliński et al., 2022a; Pasledni et al., 2022; Pałko et al., 2024; Pasledni et al., 2024), będącego hybrydowym modelem fizyczno-numerycznym. Model hybrydowy łączy w sobie podstawową zaletę modelu fizycznego, którą jest możliwość testowania fizycznej aparatury, z zaletami modeli komputerowych, w tym przede wszystkim możliwością uwzględnienia wszystkiego, co jest istotne w danym przypadku i może być opisane matematycznie.
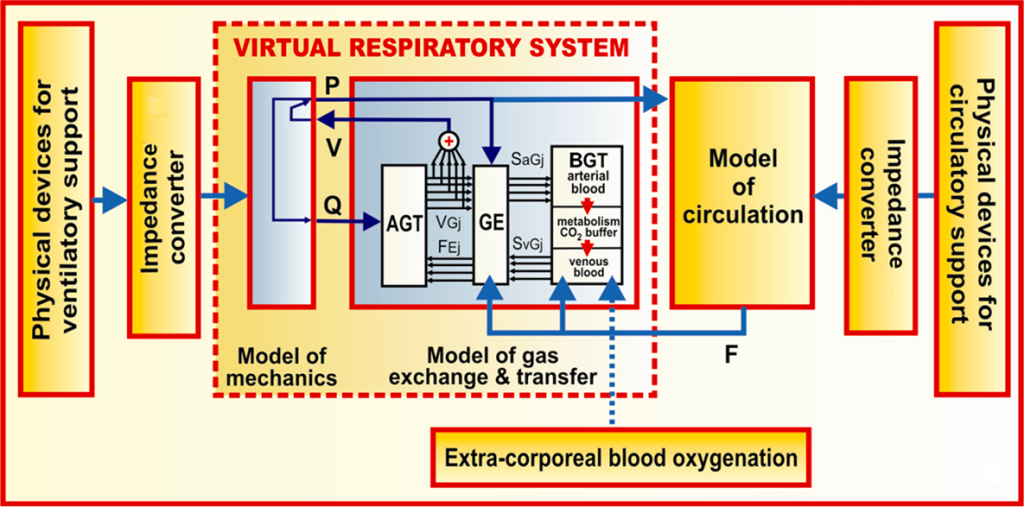
Schemat sztucznego pacjenta. AGT, GE i BGT to odpowiednio modele: transferu gazów w oskrzelach, wymiany gazowej i transportu gazów z krwią.
Nasz sztuczny pacjent krążeniowo-oddechowy to dwa sprzężone ze sobą symulatory: Hybrydowy Symulator Układu Krążenia (HSUK) oraz Hybrydowy Symulator Układu Oddechowego (HSUO). Każdy z nich składa się z dwóch zasadniczych części – numerycznego modelu oraz fizyczno-komputerowego interfejsu (Zieliński et al., 2016) będącego łącznikiem pomiędzy światem rzeczywistym reprezentowanym przez fizyczne urządzenia wspomagające (np. respirator, pompa krwi) lub diagnostyczne (np. spirometr) a światem cyfrowym reprezentowanym przez modele numeryczne. Na przestrzeni lat HSUK w różnych wersjach został sprzedany do Fundacji Rozwoju Kardiochirurgii, Akademię Górniczo-Hutniczą oraz razem z HSUO na Politechnikę Warszawską. Dodatkowo, jeden z egzemplarzy HSUK został wypożyczony na Katolicki Uniwersytet w Leuven, gdzie na podstawie umowy komercyjno-naukowej był rozwijany i wykorzystywany w ramach współpracy naukowej (Fresiello et al., 2022a, Rocchi et al., 2021, Colasanti et al., 2020), jak również oferowany jako usługa do testowania nowoopracowywanych urządzeń wspomagających pracę serca (Fresiello et al., 2022b). Egzemplarz ten po zakończeniu umowy został sprzedany Uniwersytetowi Twente.
W Pracowni powstało kilka wersji HSUO, różniących się interfejsem pneumatyczno-komputerowym, dedykowanych do różnych zastosowań: symulowania spirometrii, do symulowania układu oddechowego osoby dorosłej (Zieliński et al., 2022a) jak również pacjentów pediatrycznych oraz niemowląt (Stankiewicz et al., 2017a; Stankiewicz et al., 2017c; Stankiewicz et al., 2019a).
Cześć krążeniowa numerycznego modelu składa się z szeregu modeli o parametrach skupionych (tzw. modeli 0D) symulujących mechanikę serca oraz krążenia wieńcowego, krążenia systemowego oraz płucnego. Każdy z tych modułów wyposażony jest dodatkowo w model transportu gazów z krwią. Dodatkowo cały model układu krążenia uzupełniony jest o model metabolizmu w tkankach, autoregulacji za pomocą systemu baroreceptorów oraz modelu wazokonstrykcji płucnej.
Najbardziej zaawansowanym składnikiem numerycznym HSUO jest wirtualny układ oddechowy składający się z kilku modeli wymieniających między sobą dane; są to modele mechaniki układu oddechowego, mechaniki krążenia płucnego, transferu gazów w oskrzelach oraz wymiany gazowej oraz transportu gazów z krwią (Zieliński et al., 2019b; Zieliński et al., 2022a). Większość elementów tych modeli jest opisana nieliniowymi równaniami, w tym część parametrów równań zależy od wartości zmiennych wyliczonych przez inne modele (suplementy do Gólczewski et al., 2017; Stecka et al., 2018; Gólczewski et al., 2025). Wirtualny układ oddechowy może być również wykorzystany jako samodzielne narzędzie wykorzystywane do analizy i interpretacji zjawisk (pato)fizjologicznych obserwowanych u realnych pacjentów (e.g., Gólczewski et al., 2025).
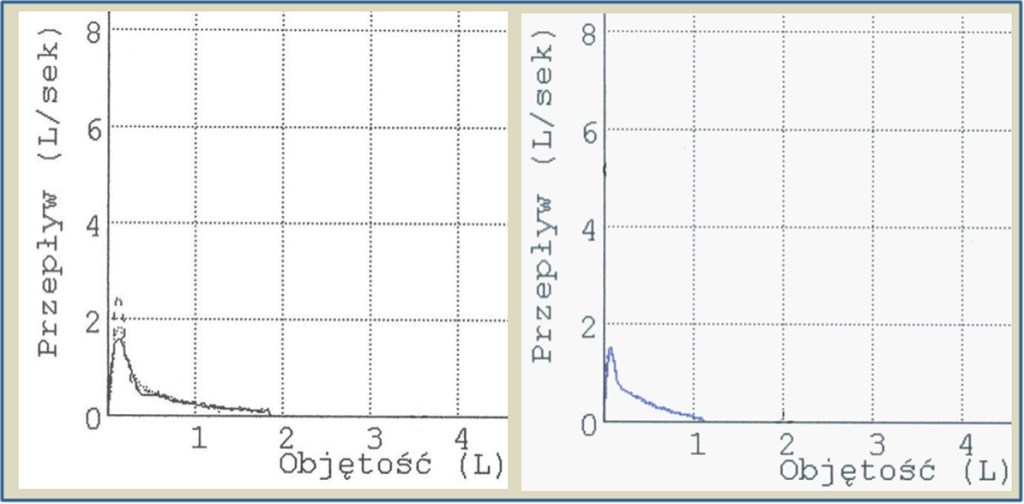
Wyniki spirometrii dwóch pacjentów z bardzo ciężką obturacyjną chorobą płuc. Jeden z tych pacjentów jest żywym pacjentem, drugi – sztucznym.
B. Mechaniczne wspomaganie układu oddechowego
Prace związane z mechanicznym wspomaganiem układu oddechowego, zarówno inżynierskie jak i badawcze, stanowią najważniejszą część aktywności Pracowni. Jednym z naszych ostatnich osiągnięć jest konstrukcja i komercjalizacja pneumatycznego dzielnika oddechowego (VENTIL) umożliwiającego wentylację każdego z płuc w różny sposób za pomocą jednego respiratora. VENTIL dzieli mieszankę oddechową, dostarczaną przez respirator do każdego z płuc osobno, według zadanej proporcji. Działania naszej Pracowni, we współpracy z Instytutem Techniki i Aparatury Medycznej Sieci Badawczej Łukasiewicz (Ł-ITAM) (obecnie część Krakowskiego Instytutu Technologicznego), zaowocowały wyprodukowaniem 200 szt. urządzania oraz wprowadzeniem go do obrotu jako wyrobu medyczny (Ł-ITAM jako producent).
Właściwości tego dzielnika zostały wykorzystane podczas pandemii COVID-19 do przetestowania koncepcji wentylacji dwóch pacjentów za pomocą jednego respiratora, co było odpowiedzią na ówczesny problem z niedoborem respiratorów. Prowadziliśmy badania zarówno laboratoryjne jak i na dużym modelu zwierzęcym (Zieliński et al., 2022b). Wyniki pokazały, że możliwe jest bezpieczne wentylowanie dwóch pacjentów przez przynajmniej 24 godziny. Taki niestandardowy rodzaj terapii oddechowej wiąże się jednak z wieloma wyzwaniami, takimi jak np. odpowiedni dobór alarmów na respiratorze czy zapewnienie dodatkowego monitorowania parametrów oddechowych każdego z wentylowanych pacjentów.
Wśród innych prac związanych z niezależną wentylacją płuc można wymienić:
- prace symulacyjne na fizycznym modelu drzewa oskrzelowego wydrukowanym przez drukarkę 3D (Kramek-Romanowska et al., 2021);
- ocena skuteczności współpracy urządzenia VENTIL z respiratorem pracującym w trybie kontrolowanego ciśnienia;
- badanie, w układzie składającym się z respiratora, VENTIL-a i dwóch sztucznych pacjentów, zaburzeń ciśnienia w drogach oddechowych jednego z pacjentów wywołanych przez takie czynniki jak np. kaszel drugiego.

Urządzenie VENTIL – nowa wersja wyprodukowana przez Ł-ITAM (obecnie część KIT)
Jednym z celów naukowych jest poszerzenie wiedzy na temat czynników ryzyka urazów płuc spowodowanych użyciem respiratora (Ventilatory Inducted Lung Injury – VILI), tj. ryzyka barotraumy, volutraumy, biotraumy lub ergotraumy. Rezultaty tych badań mają na celu wskazanie, jakie metody wentylacji lub jakie nastawy respiratora pozwalają zmniejszyć to ryzyko. VILI może być efektem źle dobranych parametrów mechanicznej wentylacji, takich jak zbyt wysokie maksymalne ciśnienie wdechowe czy zbyt duża objętość oddechowa. Ze względu na właściwości lepko-sprężyste płuc, ryzyko VILI zależy również od wielkości natężenia przepływu wdechowego mieszanki oddechowej. Oznacza to, że moc wdechowa, zdefiniowana jako iloczyn ciśnienia i przepływu wdechowego, powinna być dobrym wskaźnikiem ryzyka wystąpienia VILI, a optymalna metoda wentylacji powinna dostarczać żądaną objętość mieszanki oddechowej do płuc do przy minimalnej mocy wdechowej. Prowadzimy odpowiednie badania symulacyjne za pomocą naszego hybrydowego symulatora układu oddechowego sprzężonego z własnym pre-prototypem respiratora umożliwiającym ww. optymalną wentylację.
C. Wspomaganie diagnozowania i terapii oddechowej dzieci
Mechaniczna wentylacja dzieci wiąże się z wysokim ryzykiem urazu płuc. Dotyczy to zwłaszcza niemowląt z niehomogenicznością płuc spowodowaną wrodzoną przepukliną przeponową (CDH), wcześniactwem lub dysplazją oskrzelowo-płucną. Nasze badania ukierunkowane są na optymalizację wentylacji poprzez zindywidualizowane podejście do terapii wentylacyjnej, oparte na wcześniejszej diagnozie stopnia niehomogeniczności wentylacji. W tym celu, można wykorzystać stosunek stałych czasowych obu płuc τ1/τ2 ze względu na jego istotne korelacje z ważnymi parametrami wentylacji: szczytowym ciśnieniem wdechu, średnim ciśnienie w drogach oddechowych, pracy oddechowej i impedancji układu oddechowego (Stankiewicz et al., 2022a; Stankiewicz et al., 2021a).
Badania z wykorzystaniem symulatora oddechowego i respiratora ujawniły czynniki ryzyka związane z występowaniem niehomogeniczności wentylacji u dzieci z jednostronną CDH: szczytowe ciśnienia w bardziej hipoplastycznym płucu o mniejszej podatności mogą osiągnąć niebezpiecznie wysokie wartości grożące barotraumą, natomiast w drugim płucu może wystąpić wysoki auto-PEEP. Nasze wyniki wyjaśniają, dlaczego w ciężkich przypadkach CDH efektywną i bezpieczną może być jedynie wentylacja wysokoczęstotliwościowa (Stankiewicz et al., 2019b). Przedmiotem naszych badań było też porównanie efektywności różnych trybów wentylacji konwencjonalnej i strategii (normokapnii i permisywnej hiperkapnii), w warunkach gdy podatność układu oddechowego dziecka jest zbliżona jest do podatności wewnętrznej układu respiratora, np. u noworodków, wcześniaków (Stankiewicz et al., 2019a).
Symulacje komputerowe dotyczące wpływu wcześniactwa, dysplazji oskrzelowo-płucnej i niehomogeniczności płuc na impedancję układu oddechowego podczas oddychania spontanicznego wykazały również, że podwyższony opór dróg oddechowych i obniżona podatność układu oddechowego u wcześniaków o bardzo niskiej i ekstremalnie niskiej masie urodzeniowej skutkowały istotnym wzrostem impedancji układu oddechowego w stosunku do obserwowanej u niemowląt urodzonych o czasie (Stankiewicz et al., 2017b).
We współpracy z lekarzami zajmujemy się również badaniem wpływu anestetyków na parametry oddechowe i hemodynamiczne u dzieci podczas zabiegów operacyjnych (Kaszyński et al., 2022; Kaszyński et al., 2025). Przewodnim celem tych prac jest ograniczenie użycia leków opioidowych, poprzez zastosowanie leków znieczulających z innej grupy, jak np. lidokaina, która obecnie nie jest rutynowo stosowana u dzieci, w odróżnieniu od osób dorosłych.
W efekcie prowadzonych prac powstał też komputerowy system do diagnozy i terapii zaburzeń oddechowych w jąkaniu w postaci gry komputerowej. Na opracowane rozwiązania uzyskaliśmy dwa patenty. Wyniki badań osób jąkających się wskazują, że mówienie z zastosowaniem wizualnego sprzężenia zwrotnego, opartego na obserwacji sygnału wydychanego CO2 istotnie poprawia zarówno ergonomię oddychania podczas mówienia jak i płynność wypowiedzi (Stankiewicz et al. 2015).
D. Toracenteza
Prace dotyczące analiz i interpretacji zjawisk fizjologicznych u pacjentów z wysiękiem opłucnowym oraz zmian spowodowanych ewakuacją płynu opłucnowego są prowadzone w ścisłej współpracy z lekarzami z Warszawskiego Uniwersytetu Medycznego od 2011 r. Zostały one zapoczątkowane propozycją zbudowania specjalnego manometru do pomiaru ciśnienia w jamie opłucnej (Krenke et al., 2011). Kolejnym krokiem było zbudowanie złożonego systemu pomiarowego, w skład którego wchodził zarówno ten manometr jak i trzy komercyjne urządzenia (spirometr dostosowany przez producenta do naszych potrzeb, urządzenie do przezskórnego pomiaru gazów krwi oraz monitor kardiologiczny). System ten umożliwił pomiar wielu parametrów w trakcie toracentezy terapeutycznej (tj. ewakuacji płynu), które mogły być zsynchronizowane dzięki zastosowaniu mechanicznej quasi-delty Diraca i zapisane w komputerze.
Płyn opłucnowy powoduje zgniecenie części płuca (a nawet całego płuca w przypadku masowego wysięku). Po usunięciu płynu opłucnowego ta cześć może się rozprężyć lub nie. Najważniejszym problemem medycznym związanym z toracentezą jest niebezpieczeństwo nadmiernego spadku ciśnienia w klatce piersiowej, gdy zapadnięte płuco nie rozpręży się i miejsce po usuniętym płynie opłucnowym zostanie wypełnione ‘niczym’. Taki nadmierny spadek ciśnienia grozi między innymi obrzękiem płuc lub pęknięciem pęcherzyków w innych częściach płuc prowadząc do odmy. Stąd kluczowa choć nie zawsze doceniana rola manometrii opłucnowej.
Naszym pierwszym i to zaskakującym rezultatem była obserwacja sugerująca, że kaszel w trakcie toracentezy, który był zazwyczaj traktowany jako przeszkoda w prowadzeniu zabiegu a nawet powód do jego przerwania, wcale taki nie musi być (Zielińska-Krawczyk et al., 2015). Zostało to zweryfikowane później na znacznie większej grupie pacjentów (Stecka et al., 2022).
Możliwość pomiaru i rejestracji dokładnych wartości chwilowych ciśnienia opłucnowego pozwoliła na odkrycie pulsowania ciśnienia opłucnowego (Grabczak et al., 2020) czy też analizę zmian amplitudy fluktuacji ciśnienia opłucnowego związanych z oddychaniem (Zielińska-Krawczyk et al., 2018). Pomiar innych parametrów pozwolił na dalsze analizy (Zielińska-Krawczyk et al., 2022).
Istotną częścią badań związanych z toracentezą było wykorzystanie naszego uniwersalnego wirtualnego pacjenta (Zieliński et al., 2019b; Zieliński et al., 2022) w interpretacji zaobserwowanych zjawisk, czasem zaskakujących jak na przykład brak wpływu nawet masowego wysięku na gazometrię krwi tętniczej, mimo że taki wysięk istotnie zaburza oddychanie (Stecka et al., 2018; Gólczewski et al., 2025).
Prace w tym zakresie są w dalszym ciągu kontynuowane, zarówno jeśli chodzi o badanie nowej grupy pacjentów jak i o nowe analizy, np. nowe wyjaśnienie przyczyny duszności będącej podstawowym a czasem jedynym objawem zgłaszanym przez pacjentów z wysiękiem opłucnowym.
Mając doświadczenie w budowaniu manometrów do biopomiarów, stworzyliśmy również manometr do pomiaru ciśnienia w ustach niemowląt w trakcie ssania i przeprowadziliśmy wstępne badania (Czajkowska et al., 2019).
E. Rola odbić fal pulsu w fizjologii i psychologii
Uogólnione sztywnienie tętnic jest podstawowym, fizjologicznym efektem procesu starzenia się układu krążenia. Wzrost sztywności tętnic powoduje zmniejszenie się odbić fal przepływu i ciśnienia od oporów obwodowych. W skrajnym przypadku mogłoby dojść do tzw. dopasowania falowego, tj. do sytuacji, w której opór sprężysty tętnic, niski u osób młodych, wzrósłby na tyle, że zrównałby się z oporem obwodowym, co doprowadziłoby do zaniku odbić. Zrównanie oporu sprężystego tętnic z oporem obwodowym może też nastąpić w przypadku znacznego spadku tego drugiego, spowodowanego np. wazodylatacją metaboliczną lub lekami p/nadciśnieniowymi.
Choć w technice zazwyczaj dąży się do dopasowania falowego, to jednak w przypadku układu krążenia doprowadziłoby ono do śmierci organizmu, bowiem z powodu braku odbić, cała porcja krwi wstrzykiwana przez serce w okresie skurczu przechodziłaby przez mikrokrążenia w tym okresie, w efekcie czego ciśnienie rozkurczowe byłoby równe zeru, co powodowałoby niedokrwienia organizmu w okresie rozkurczy. Wzrost oporów obwodowych u osób starszych ze zwiększonym oporem sprężystym tętnic może więc być traktowany jako swego rodzaju mechanizm obronny, mimo że prowadzi do nadciśnienia tętniczego.
Wielkość odbić, czyli swego rodzaju odległość od dopasowania falowego, determinuje kształt krzywej będącej wykresem wielkości przepływu krwi w danym miejscu (np. w tętnicy ramiennej lub szyjnej) w funkcji czasu. W Pracowni opracowano taką matematyczną metodę ilościowego opisu tego kształtu za pomocą jednego wskaźnika, że wartość tego wskaźnika jest ściśle skorelowana z wiekiem. Dzięki odpowiedniej standaryzacji tego wskaźnika za pomocą regresji liniowej, jego wartość dla przeciętnej, zdrowej i wypoczętej osoby w danym wieku jest równa temu wiekowi; stąd nazwa wskaźnika: ‘wiek krzywej’ (waveform age – WA).
Ponieważ zbliżenie się do dopasowania falowego jest niekorzystne dla organizmu, aktywność fizyczna wymagająca obniżenia wartości oporów obwodowych jest ograniczona przez procesy usztywniające tętnice. Jeśli uznać, że stan fizyczny organizmu ma wpływ na procesy psychiczne, ograniczenie to dotyczy również aktywności psychicznej. Zarówno analizy teoretyczne jak i pomiary WA w różnych grupach osób pozwoliły wytłumaczyć wiele kwestii, np. dlaczego leczenie p/nadciśnieniowe części osób w zaawansowanym wieku prowadzi do zachowań depresyjnych i dlaczego umiarkowane nadciśnienie rozkurczowe jest związane z zwiększą przeżywalnością osób starszych (Gólczewski, 2021). Wydaje się jednak, że z poznawczego punktu widzenia najciekawsze są związki WA, tj. wielkości odbić fal pulsu, z właściwościami psychicznymi, w tym z Ilorazem Inteligencji (Gólczewski, 2021) i tzw. mgłą mózgową będącą długotrwałym powikłaniem COVID-19 (Gólczewski et al., 2024).
F. Spirometria
W przeszłości, jednym z wiodących tematów w Pracowni były badania związane ze spirometrią i innymi sposobami oceny oporów dróg oddechowych oraz elastyczności płuc. Badania te obejmowały zarówno analizy danych pozyskanych od realnych pacjentów (we współpracy z Wojskowym Instytutem Medycznym) jak i analizy teoretyczne, w tym przy wykorzystaniu naszego wirtualnego lub sztucznego (hybrydowego) pacjenta (Zieliński et al., 2019b; Zieliński et al., 2022a).
Ostatnia analiza danych realnych pacjentów dotyczyła istotnych różnic, w wartościach indeksów spirometrycznych, między bazami danych stworzonych pod koniec XX i w XXI wieku. Dodatkowo okazało się, że spirometryczne równania predykcyjne ECSC, opracowane na podstawie danych zebranych w Europie Zachodniej w latach 70. XX w., już nie były odpowiednie dla populacji z tamtej części Europy w latach 90. i dla populacji polskiej w XXI w., ale były odpowiednie dla polskiej populacji w latach 90. XX w. Te porównania i konfrontacja ze zmianami spodziewanej długości życia w Polsce i krajach Europy Zachodniej pozwoliły zasugerować konieczność periodycznej aktualizacji równań predykcyjnych w miarę rozwoju społeczno-ekonomicznego danej populacji (Chciałowski et al., 2019).
Wykorzystując sztucznego pacjenta pokazano, jak zmienione właściwości elastyczne płuc mogą zafałszować diagnozę chorób obturacyjnych, jeśli bazuje się wyłącznie na wynikach badania spirometrycznego (Pałko et al., 2020).
Nagrody
- Prix Galien’2012 (Złoty medal w kategorii „Innowacyjna praca badawcza”) za: Oryginalny sztuczny pacjent oddechowo-krążeniowy
- Złoty Skalpel’2018 (Miejsce VII) za: Zastosowanie elektronicznej manometrii opłucnowej w wysokoobjętościowej toracentezie, kwalifikacji do pleurodezy i poznawaniu procesów patofizjologicznych zachodzących w jamie opłucnowej.
- Polski Produkt Przyszłości’2021 (Nagroda w kategorii „Produkt Przyszłości Instytucji Szkolnictwa Wyższego i Nauki”) za: VENTIL – innowacyjne urządzenie do niezależnej wentylacji płuc
- Nagroda gospodarcza Prezydenta RP’2021 (w kategorii „Badania+Rozwój)
Współpraca w ostatnich 10 latach
- Warszawski Uniwersytet Medyczny (prof. Rafał Krenke; dr Magdalena Mierzewska-Schmidt)
- Wojskowy Instytut Medyczny (prof. Andrzej Chciałowski)
- Instytut Techniki i Aparatury Medycznej Sieci Badawczej Łukasiewicz (obecnie część Krakowskiego Instytutu Technologicznego)
- Instytut Fizjologii Klinicznej Włoskiej Akademii Nauk (dr Gianfranco Ferrari)
- Katolicki Uniwersytet w Leuven (dr Libera Fresiello)
- Politechnika Bydgoska (prof. Tomasz Topoliński)
- Szkoła Główna Gospodarstwa Wiejskiego (prof. Zdzisław Gajewski)
Projekty zewnętrzne w ostatnich 10 latach
- Projekt badawczy NCN OPUS Nr 2012/05/B/NZ5/01343 „Czynność wentylacyjna płuc, wskaźniki wymiany gazowej i reakcja układu krążenia w warunkach zmian ciśnienia śródopłucnowego wywołanych terapeutyczną punkcją opłucnej”.
- Projekt badawczy NCN OPUS Nr 2019/35/B/NZ5/02531 „Wykorzystanie wysokoobjętościowej toracentezy i pomiaru ciśnienia opłucnowego do badania nowo opisanych zjawisk patofizjologicznych u chorych z płynem w jamie opłucnej”.
- Projekt badawczy NCBR LIDER Nr UMO-LIDER/19/0107/L-8/16/NCBR/2017 „System do niezależnej wentylacji płuc z funkcją podawania leków inhalacyjnych”.
- Projekt Badawczy NCN SONATA Nr 2021/43/D/ST7/01912 „Ocena efektywności działania systemu do niezależnej wentylacji płuc wraz z respiratorem pracującym w trybach kontrolowanego ciśnienia”.
- Projekt badawczy NCN MAESTRO Nr 2023/50/A/ST7/00498 „Opracowanie optymalnej wentylacji płuc minimalizującej ryzyko urazu płuc wywołanego respiratorem (VILI)”.
- Projekt wymiany dwustronnej w ramach współpracy pomiędzy Polską Akademią Nauk a Fundacją Badawczą Flandria „Symulator układu krążenia do testowania urządzeń wspomagających”.
Patenty w ostatnich 10 latach
Europejskie:
- Darowski M, Kozarski M, Stankiewicz B, Michnikowski M, Pałko KJ, Zieliński K. Volume divider and method of respiratory gas division. EP3154617 (2020).
Polskie:
- Darowski M, Kozarski M. Sposób oraz system do sterowania objętością wdechowej mieszanki gazowej pacjenta dostarczonej przez rozdzielenie wdechowej mieszanki gazowej respiratora do co najmniej jednego z dwóch torów oddechowych z pojedynczego respiratora oraz powiązany sposób oraz system do wielostanowiskowej wentylacji wdechową mieszanką gazową respiratora z pojedynczego respiratora. PL245364 (2024).
- Darowski M, Kozarski M. Płynowoelektryczny transformator impedancji oraz sposób równoważenia mocy w płynowoelektrycznym transformatorze impedancji. PL246699 (2024).
- Darowski M, Kozarski M. Modułowy system wielostanowiskowej wentylacji płuc. PL244255 (2023).
- Darowski M, Kozarski M. Głowica pomiarowa strumienia gazu oddechowego. PL244335 (2023).
- Kozarski M, Darowski M, Zieliński K, Kozarski Ł. Interfejs hybrydowy do badań pompy balonowej. PL237195 (2020).
- Kozarski M, Darowski M, Zieliński K. Anemometryczny różnicowy czujnik strumienia gazu. PL226850 (2018).
- Kozarski M, Darowski M, Zieliński K. Sposób pomiaru mechanicznych parametrów układu oddechowego. PL 229751 (2018).
- Kozarski M, Darowski M, Zieliński K. Pojemnościowy czujnik przemieszczenia. PL226850 (2017).
- Kozarski M, Darowski M, Pałko KJ, Zieliński K. Sposób i urządzenie do wspomagania oddechu pacjenta. PL227710 (2017).
- Kozarski M, Darowski M, Pałko KJ, Zieliński K. Dawkująco-mierzący mieszacz gazów oddechowych. PL223585 (2016).
- Kozarski M, Darowski M, Pałko KJ, Zieliński K. Indukcyjnościowy czujnik przemieszczeń. PL 223714 (2016).
- Kozarski M, Darowski M, Pałko KJ, Zieliński K. Objętościomierz dwunurnikowy. PL223960 (2016).
- Kozarski M, Darowski M, Zieliński K, Pałko KJ, Górczyńska K. Układ hybrydowy do badania pomp wirnikowych. PL 223018 (2015).
- Darowski M, Kozarski M, Stankiewicz B, Michnikowski M, Pałko KJ, Zieliński K. Automatyczny dzielnik objętości mieszanki gazu wdechowego. PL 221432 (2015).
- Kozarski M, Darowski M, Zieliński K. Intubacyjny czujnik ciśnienia. PL221385 (2015).
Publikacje w ostatnich 10 latach
- Chciałowski A, Gólczewski T. (2019). Spirometry: A need for periodic updates of national reference values. Adv Exp Med Biol. 1222:1-8. https://doi.org/10.1007/5584_2019_432
- Colasanti S, Piemonte V, Devolder E, Zieliński K, Vandendriessche K, Meyns B, Fresiello L. (2021). Development of a computational simulator of the extracorporeal membrane oxygenation and its validation with in vitro measurements. Artif Organs 45, 399–410. https://doi.org/10.1111/aor.13842
- Czajkowska M, Fonfara A, Królak-Olejnik B, Michnikowski M, Gólczewski T. (2019). The impact of early therapeutic intervention on the central pattern generator in premature newborns – a preliminary study and literature review. Developmental period medicine, 23(3), 178–183. https://doi.org/10.34763/devperiodmed.20192303.178183
- Fresiello L, Zieliński K. (2020). Hemodynamic Modelling and Simulations for Mechanical Circulatory Support, in: Karimov, J.H., Fukamachi, K., Starling, R.C. (Eds.), Mechanical Support for Heart Failure : Current Solutions and New Technologies. Springer International Publishing, Cham, pp. 429–447. https://doi.org/10.1007/978-3-030-47809-4_26
- Fresiello L, Muthiah K, Goetschalck K, Hayward C, Rocchi M, Bezy M, Pauls JP, Meyn, B, Donke, DW, Zieliński K. (2022a). Initial clinical validation of a hybrid in silico-in vitro cardiorespiratory simulator for comprehensive testing of mechanical circulatory support systems. Front Physiol 13, 967449. https://doi.org/10.3389/fphys.2022.967449
- Fresiello L, Najar A, Brynedal Ignell N, Zieliński K, Rocchi M, Meyns B, Perkins IL. (2022b). Hemodynamic characterization of the Realheart® total artificial heart with a hybrid cardiovascular simulator. Artif Organs 46, 1585–1596. https://doi.org/10.1111/aor.14223
- Gólczewski T, Stecka A M, Michnikowski M, Grabczak E M, Korczyński P, Krenke R. (2017). The use of a virtual patient to follow pleural pressure changes associated with therapeutic thoracentesis. Int J Artif Organs, 40(12), 690–695. https://doi.org/10.5301/ijao.5000636
- Gólczewski T. (2021) Arterial blood flow waveform shapes – their original quantification and importance in chosen aspects of physiology and psychology: A review. Biocybern Biomed Eng, 41:1418-1435 https://doi:10.1016/j.bbe.2021.04.007
- Gólczewski T, Plewka K, Michnikowski M, Chciałowski A. (2024). Correlations between vascular properties and mental dysfunctions in long-COVID-19 support the vascular depression hypothesis. Biocybern Biomed Eng, 44(3):461-469. https://doi.org/10.1016/j.bbe.2024.07.001
- Gólczewski T, Stecka AM, Grabczak EM, Michnikowski M, Zielińska-Krawczyk M, Krenke R. (2025). Hemidiaphragm work in large pleural effusion and its insignificant impact on blood gases: a new insight based on in silico study. Front Physiol, 16:1539781 https://doi:10.3389/fphys.2025.1539781
- Grabczak EM, Michnikowski M, Styczynski G, Zielinska-Krawczyk M, Stecka AM, Korczynski P, Zielinski K, Palko KJ, Rahman NM, Golczewski T, Krenke R. (2020). Pleural pressure pulse in patients with pleural effusion: A new phenomenon registered during thoracentesis with pleural manometry. J Clin Med, 9(8), 2396. https://doi.org/10.3390/jcm9082396
- Kaszyński M, Stankiewicz B, Pałko KJ, Darowski M, Pągowska-Klimek I.(2022) Impact of lidocaine on hemodynamic and respiratory parameters during laparoscopic appendectomy in children. Sci Rep 18;12(1):14038. https://doi.org/10.1038/s41598-022-18243-3
- Kaszyński M, Kuczerowska A, Pietrzyk J, Sawicki P, Witt P, Stankiewicz B, Darowski M, Pągowska-Klimek I. (2025). Influence of intravenous lidocaine infusion on haemodynamic response to tracheal intubation and metabolic-hormonal responses during laparoscopic procedures in children: a randomised controlled trial. BMC Anesthesiol 25;23. https://doi.org/10.1186/s12871-024-02885-z
- Kozarski M, Suwalski P, Zieliński K, Górczyńska K, Szafron B, Pałko KJ, Smoczyński R, Darowski M. (2015). A hybrid (hydro-numerical) circulatory model: investigations of mechanical aortic valves and a numerical valve model. Bull Pol Acad Sci Tech Sci 63, 605–612. https://doi.org/10.1515/bpasts-2015-0071
- Kramek-Romanowska K, Stecka AM, Zieliński K, Dorosz A, Okrzeja P, Michnikowski M, Odziomek M. (2021). Independent Lung Ventilation-Experimental Studies on a 3D Printed Respiratory Tract Model. Materials (Basel) 14, 5189. https://doi.org/10.3390/ma14185189
- Krenke R, Guć M, Grabczak E M, Michnikowski M, Pałko K J, Chazan R, Gólczewski T. (2011). Development of an electronic manometer for intrapleural pressure monitoring. Respiration, 82(4), 377–385. https://doi.org/10.1159/000328718
- Pałko KJ, Gólczewski T, Kozarski M, Stankiewicz B, Darowski M. (2020). A New Method and Device for Differentiating Elastic and Resistive Properties of the Respiratory System. In: Korbicz, J., Maniewski, R., Patan, K., Kowal, M. (eds) Current Trends in Biomedical Engineering and Bioimages Analysis. PCBEE 2019. Advances in Intelligent Systems and Computing, vol 1033. Springer, Cham. https://doi.org/10.1007/978-3-030-29885-2_4
- Pałko KJ, Kołodziej D, Darowski M. (2024) Lung divisions for models of cardiopulmonary interaction – preliminary tests. Pol J Med Phys Eng 30(2), 52-68. https://doi.org/10.2478/pjmpe-2024-0007
- Pasledni R, Zieliński K. (2022). Hybrid Cardiovascular Simulator – An Application for the Mechanical Assistance by an Intra-aortic Balloon Pump, in: Pijanowska, D.G., Zieliński, K., Liebert, A., Kacprzyk, J. (Eds.), Biocybernetics and Biomedical Engineering – Current Trends and Challenges. Springer International Publishing, Cham, pp. 98–107. https://doi.org/10.1007/978-3-030-83704-4_10
- Pasledni R, Kozarski M, Mizerski JK, Darowski M, Okrzeja P, Zieliński K. (2024). The hybrid (physical-computational) cardiovascular simulator to study valvular diseases. J Biomech. 170, 112173. https://doi.org/10.1016/j.jbiomech.2024.112173
- Rocchi M, Fresiello L, Meyns B, Jacobs S, Gross C, Pauls JP, Graefe R, Stecka AM, Kozarski M, Zieliński K. (2021). A Compliant Model of the Ventricular Apex to Study Suction in Ventricular Assist Devices. ASAIO J 67, 1125–1133. https://doi.org/10.1097/MAT.0000000000001370
- Stankiewicz B, Zieliński K, Darowski M, Michnikowski M (2015): EtCO2-based biofeedback method of breath regulation increases speech fluency of stuttering people. Arch Acoust 40(4):469-474.
- Stankiewicz B, Pałko K J, Darowski M, Zieliński K, Kozarski M. (2017a). A new infant hybrid respiratory simulator: preliminary evaluation based on clinical data. Med Biol Eng Comput. 55, 1937–1948 DOI:10.1007/s11517-017-1635-9.
- Stankiewicz B, Darowski M, Pałko KJ. (2017b). Influence of Preterm Birth, BPD and Lung Inhomogeneity on Respiratory System Impedance – Model Studies. In: Augustyniak P, Maniewski R, Tadeusiewicz R (eds.), Recent Developments and Achievements in Biocybernetics and Biomedical Engineering 201 (455934_1_En, Chapter 6). PCBBE 2017. Advances in Intelligent Systems and Computing, vol. 647. Springer.
- Stankiewicz B, Rawicz M, Darowski M, Zieliński K, Kozarski M, Chwojnowski A. (2017c): Use of siliconised infant endotracheal tubes reduces work of breathing under turbulent flow. Biocybern Biomed Eng 37(1):59-65. DOI:10.1016/j.bbe.2016.11.002.
- Stankiewicz B, Pałko KJ, Darowski M, Kozarski M. (2019a). How to ventilate preterm infants with lung compliance close to circuit compliance – real-time simulations on an infant hybrid respiratory simulator. Med Biol Eng Comput 58, 357–37. https://doi.org.10.1007/s11517-019-02089-5.
- Stankiewicz B, Pałko KJ, Darowski M, Kozarski M and Górczyńska K. (2019b). Challenges with conventional ventilation of infants with inhomogeneous lungs. In: Korbicz J, Maniewski R, Patan K, Kowal M (eds): Current Trends in Biomedical Engineering and Bioimages Analysis. PCBEE 2019. Advances in Intelligent Systems and Computing, vol. 1033:224-234. Springer, Cham. https://doi.org/10.1007/978-3-030-29885-2_21.
- Stankiewicz B, Mierzewska-Schmidt M., Górczyńska K, Baranowski A., Kozarski M, Darowski M (2021). Ventilation inhomogeneity in CDH infants – A new attitude within a simulation study, Biocybern Biomed Eng, 41(4):1378-1389. https://doi.org/10.1016/j.bbe.2021.08.002.
- Stankiewicz B, Mierzewska-Schmidt M, Pałko KJ, Baranowski A, Darowski M, Kozarski M. (2022). A new method of ventilation inhomogeneity assessment based on a simulation study using clinical data on congenital diaphragmatic hernia cases. Sci Rep 12:22635. https://doi.org/10.1038/s41598-022-27027-8
- Stecka AM, Gólczewski T, Grabczak EM, Zieliński K, Michnikowski M, Zielińska-Krawczyk M, Korczyński P, Krenke R. (2018). The use of a virtual patient to follow changes in arterial blood gases associated with therapeutic thoracentesis. Int J Artif Organs, 41(11), 690–697. https://doi.org/10.1177/0391398818793354
- Stecka A M, Grabczak E M, Michnikowski M, Zielińska-Krawczyk M, Krenke R, Gólczewski T. (2022). The impact of spontaneous cough on pleural pressure changes during therapeutic thoracentesis. Sci Rep, 12(1), 11502. https://doi.org/10.1038/s41598-022-15480-4
- Zielinska-Krawczyk M, Michnikowski M, Grabczak E M, Palko K J, Korczynski P, Golczewski T, Krenke R. (2015). Cough during therapeutic thoracentesis: friend or foe?. Respirology 20(1), 166–168. https://doi.org/10.1111/resp.12426
- Zielinska-Krawczyk M, Grabczak E M, Michnikowski M, Zielinski K, Korczynski P, Stecka A, Golczewski T, Krenke R. (2018). Patterns of pleural pressure amplitude and respiratory rate changes during therapeutic thoracentesis. BMC Pulm Med 18(1), 36. https://doi.org/10.1186/s12890-018-0595-7
- Zielinska-Krawczyk M, Stecka AM, Grabczak EM, Michnikowski M, Zieliński K, Korczynski P, Gólczewski T, Krenke R. (2022). Impact of therapeutic thoracentesis and pleural pressure changes on breathing pattern, dyspnea, lung function, and arterial blood gases. Pol Arch Intern Med. 132(4):16185. https://doi:10.20452/pamw.16185
- Zieliński K, Darowski M, Kozarski M, Ferrari G. (2016). The need for hybrid modeling in analysis of cardiovascular and respiratory support. Int J Artif Organs 39, 265–271. https://doi.org/10.5301/ijao.5000513
- Zieliński K, Okrzeja P, Stecka A, Kozarski M, Darowski M. (2019a). A Hybrid Cardio-Pulmonary Simulation Platform—An Application for Extracorporeal Assist Devices. In: Lhotska, L., Sukupova, L., Lacković, I., Ibbott, G.S. (eds) World Congress on Medical Physics and Biomedical Engineering 2018. IFMBE Proceedings, vol 68/1. Springer, Singapore. https://doi.org/10.1007/978-981-10-9035-6_130
- Zieliński K, Stecka A, Gólczewski T. (2019b). VirRespir—An Application for Virtual Pneumonological Experimentation and Clinical Training. In: Lhotska, L., Sukupova, L., Lacković, I., Ibbott, G.S. (eds) World Congress on Medical Physics and Biomedical Engineering 2018. IFMBE Proceedings, vol 68/1. Springer, Singapore. https://doi.org/10.1007/978-981-10-9035-6_129
- Zieliński K, Górczyńska K, Kozarski M, Okrzeja P, Darowski M, Ferrari G. (2020). A Novel Real-Time Computer Model of the Coronary System Including a Physiological Feedback Between the Left Ventricular Muscles and Coronary Perfusion, in: Korbicz, J., Maniewski, R., Patan, K., Kowal, M. (Eds.), Current Trends in Biomedical Engineering and Bioimages Analysis. Springer International Publishing, Cham, pp. 265–276. https://doi.org/10.1007/978-3-030-29885-2_24
- Zieliński K, Gólczewski T, Kozarski M, Darowski M. (2022a). Virtual and Artificial Cardiorespiratory Patients in Medicine and Biomedical Engineering. Membranes, 12(6), 548. https://doi.org/10.3390/membranes12060548
- Zieliński K, Lisowska B, Siewruk K, Sady M, Ferenc K, Barwijuk M, Olszewski J, Anusz K, Jabłoński A, Gajewska M, Okrzeja P, Michnikowski M., Pijanowska, D.G., Pluta, K., Remiszewska, E., Darowski M, Zabielski R, Liebert A., Kramek-Romanowska, K., Stecka A, Kozarski M, Pasledni R, Gajewski Z, Ładyżyński P. (2022b). Automatic air volume control system for ventilation of two patients using a single ventilator: a large animal model study. Sci Rep 12, 22591. https://doi.org/10.1038/s41598-022-26922-4