Pracownia Elektrostatycznych Metod Bioenkapsulacji
Kierownik Pracowni:
Dr hab. inż. Dorota Lewińska, prof. instytutu IBIB PAN
Od roku 2022, po dołączeniu do Pracowni Zespołu prof. Andrzeja Chwojnowskiego tematyka badawcza prowadzona w PEMB uległa poszerzeniu i obecnie obejmuje trzy zasadnicze tematy badawcze.
Pierwszy z nich ścisłe związany jest z wykorzystaniem impulsowego pola elektrostatycznego do wytwarzania polimerowych nośników substancji biologicznie aktywnych oraz żywych komórek. Obejmują one następujące rodzaje nośników:
Włókniny polimerowe.
Obecnie prowadzone prace obejmują między innymi badanie wpływu parametrów procesu impulsowego elektroprzędzenia na strukturę wytwarzanych włóknin. Stosując wieloparametryczną analizę czynnikową typu 23 zbadano:
- wpływ wybranych parametrów procesu elektroprzędzenia (napięcia, natężenia przepływu roztworu polimeru oraz lepkości tego roztworu) na grubość włókien i zdolność układu do wytwarzania włóknin koralikowych (ang. bead-on-string- Rys. 1a ) i jednorodnych (Rys. 1b)

Rys. 1. Zdjęcia SEM włóknin polimerowych o różnej morfologii: a) typu bead-on string, b) jednorodnych.
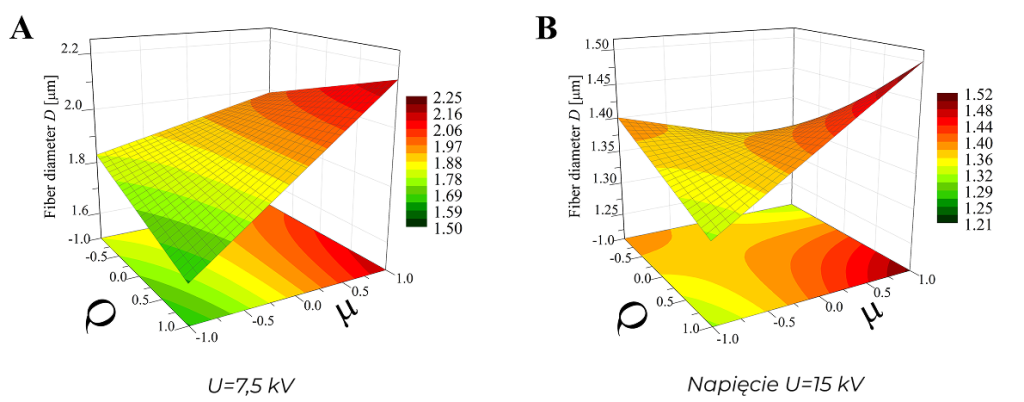
Rys. 2. Przykładowy wynik analizy czynnikowej: wykresy powierzchniowe przedstawiające wpływ wielkości natężenia przepływu roztworu polimeru Q (w zakresie 0,6-1,2 ml/h) i lepkości tego roztworu µ (w zakresie 0,043-0,107 Pa*s) na grubość włókien D dla włóknin jednorodnych, wytworzonych przy różnych wartościach napięcia U. Korycka et al. Beilstein J. Nanotechnol. 2018.
- Wpływ wielkości parametrów elektrycznych procesu elektroprzędzenia impulsowego (U, f i τ) na średnicę i morfologię mono- i bi-modalnych włóknin polimerowych.


Rys. 3. Zdjęcie SEM włókniny: a) monomodalnej o jednkowej grubości nici i b) bi-modalnej, zbudowanej z nici o różnej grubości. Bartkowiak et al. Polymers 2024.
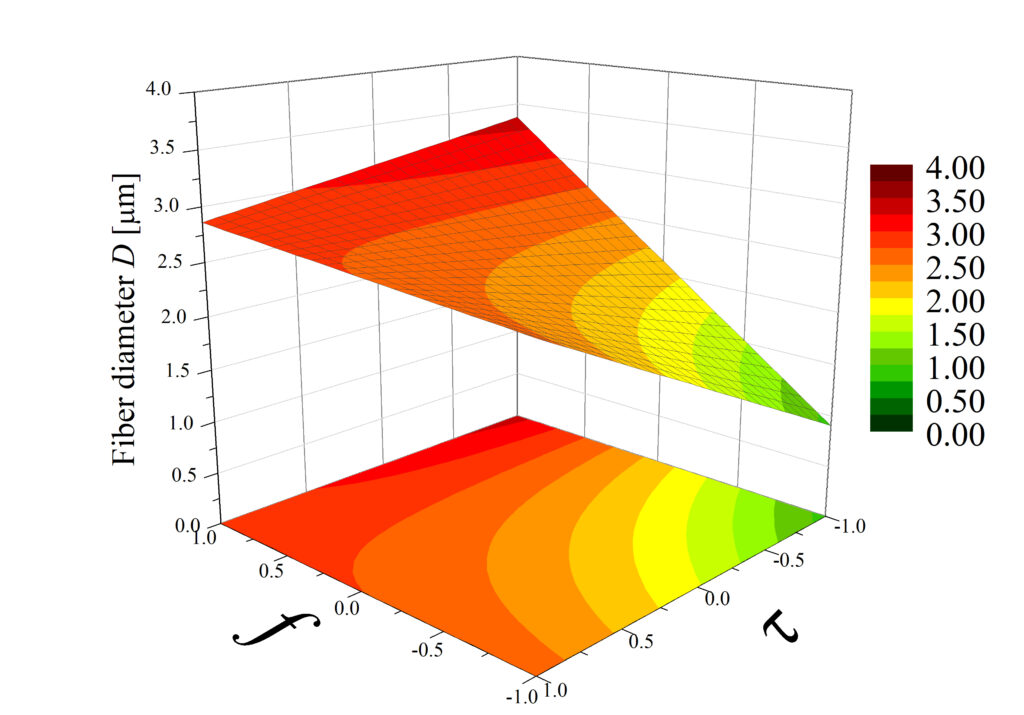
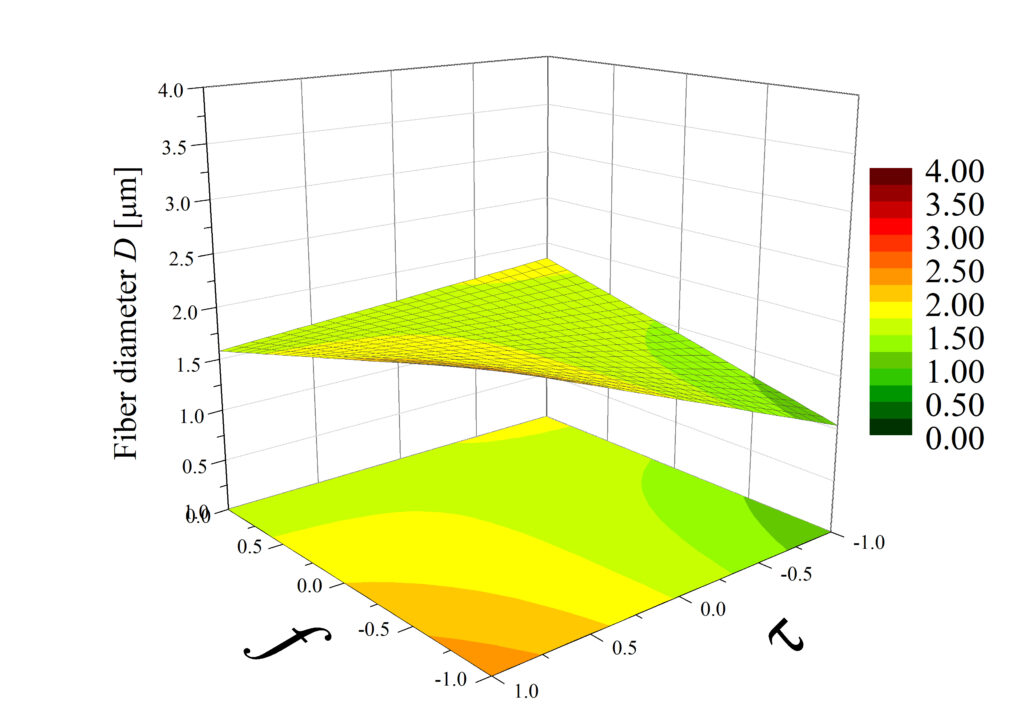
Rys. 4. Przykładowy wynik analizy czynnikowej: wykresy powierzchniowe przedstawiające wpływ częstotliwości impulsów elektrycznych f (w zakresie 30-100 Hz) i czasu trwania tych impulsów (w zakresie 1-9 ms) na grubość włókien D, wytworzonych przy różnych wartościach napięcia U. Bartkowiak et al. Polymers 2024.
Sferyczne mikrokulki polimerowe
Sferyczne mikrokulki polimerowe z polimerów syntetycznych i naturalnych przeznaczone do immobilizacji leków i żywych komórek.

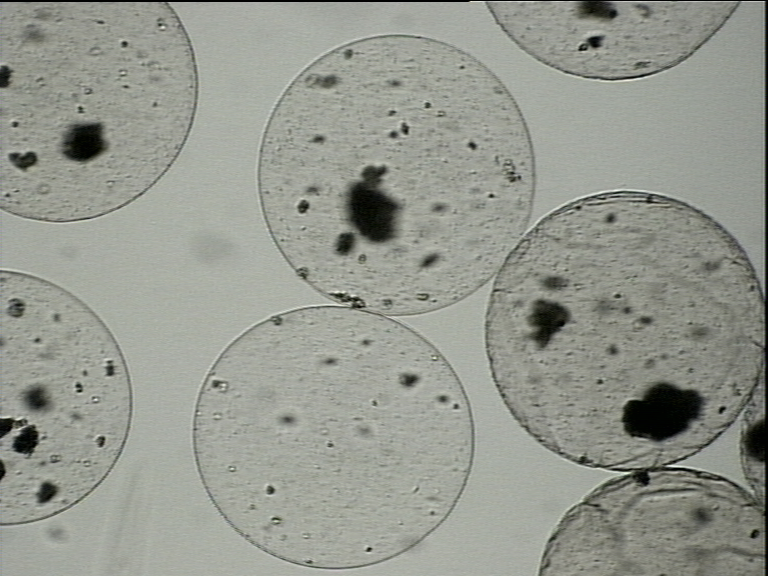
Rys. 5. Sferyczne mikromatryce polimerowe wytworzone z: a) polimeru syntetycznego Mirek et al. Colloids and Surfaces A: Physicochemical and Engineering Aspects 2022; b) polisacharydu zawierające immobilizowane komórki ludzkich przytarczyc.
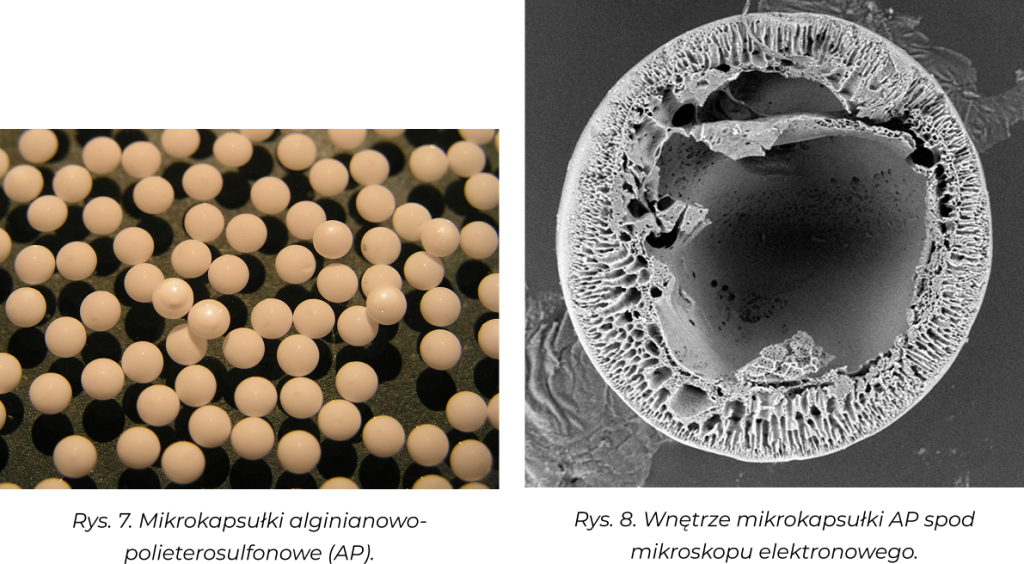
Mikrokapsułki alginianowe i alginianowo/polieterosulfonowe, przeznaczone do enkapsulacji żywych komórek, wytwarzane w procesie jednoetapowym z użyciem głowic współosiowych:
- dwudyszowej – PATENT RP Nr 208384
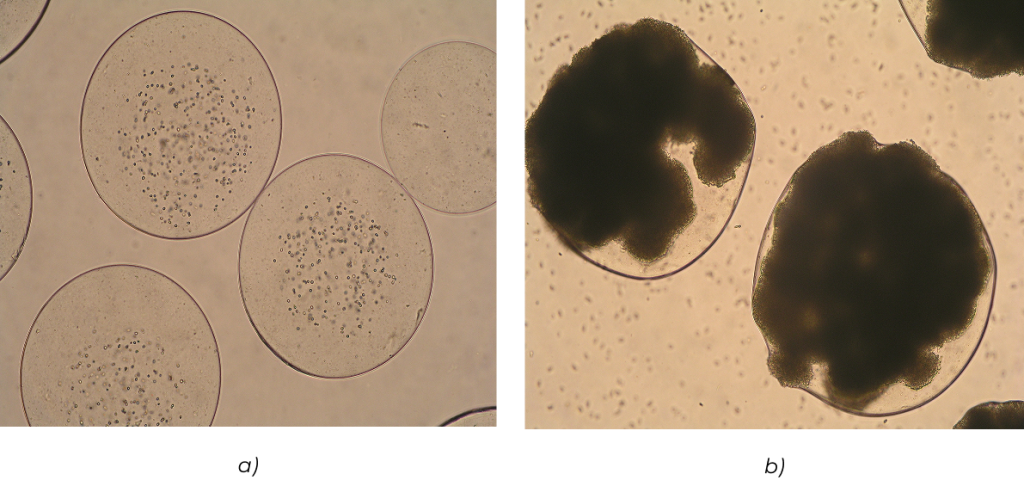
Rys. 6. Komórki drożdży piekarskich enkapsulowane wewnątrz sferycznych matryc alginianowych wytworzonych za pomocą głowicy dwudyszowej: a) bezpośrednio po wytworzeniu, b) po 48 godzinach hodowli. Lewińska et al. Biocybernetics and Biomedical Engineering, 2008, 28(2), 69-84
- trójdyszowej – (hydrożelowy rdzeń/polimerowa membrana półprzepuszczalna wykonana z polimeru syntetycznego PATENT RP Nr 208383
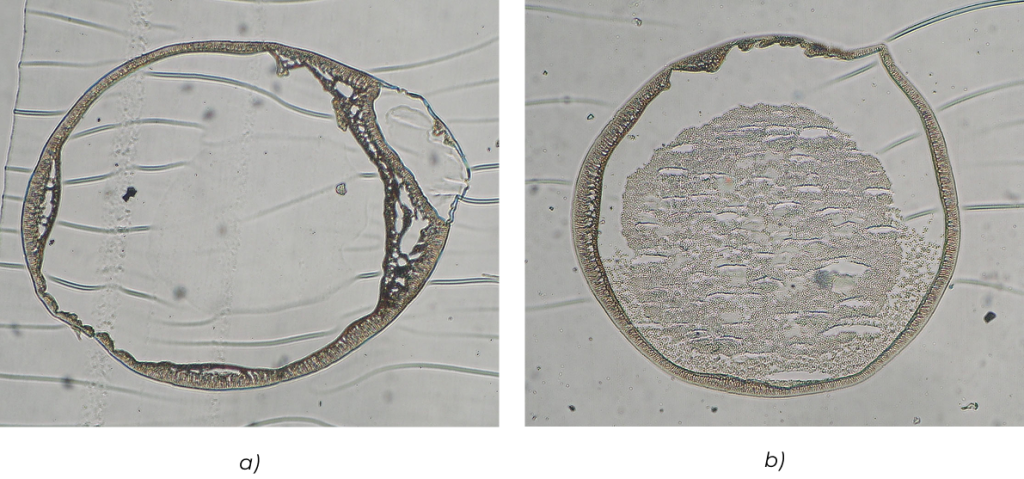
Rys. 9. Wnętrze mikrokapsułek AP zawierających enkapsulowane drożdże piekarskie: (a) przed i (b) po 24 godz. hodowli.
W Pracowni prowadzone są także prace nad opracowywaniem metod badania właściwości wytwarzanych nośników polimerowych Lewińska et al. J. Membrane Sci, Grzeczkowicz et al. Desalination and Water Treatment 2018, Kupikowska-Stobba et al. Biocybernetics and Biomedical Engineering 2021, a ostatnio także opracowywane są nowe tusze do biodruku 3D Mirek et al. Biomaterials Advances, 2023.
Słowa kluczowe: elektroprzędzenie, elektrosprying, impulsowe pole elektrostatyczne, mikrokapsułki, mikrokulki, mikroenkapsulacja komórek.
Wybranie publikacje
- Korycka P., Mirek A., Kramek-Romanowska K., Grzeczkowicz M., Lewińska D. „Effect of electrospinning process variables on the average size of polymer fibers and bead-on-string structures established with a factorial design.” Beilstein J. Nanotechnol. 2018, 9, 2466-2478
- Kramek-Romanowska K., Grzeczkowicz M., Korycka P., Lewińska D. “A Factorial Design for Assessment of the Effect of Selected Process Variables on the Impulse Electrostatic Droplet Formation.” In: Korbicz J., Maniewski R., Patan K., Kowal M. (eds) Current Trends in Biomedical Engineering and Bioimages Analysis. PCBEE 2019. Advances in Intelligent Systems and Computing, vol 1033, pp 327-336, (2020) Springer, Cham, DOI https://doi.org/10.1007/978-3-030-29885-2_30
- Bartkowiak A., Grzeczkowicz M., Lewińska D. “The Effects of Pulsed Electrospinning Process Variables on the Size of Polymer Fibers Established with a 23 Factorial Design” Polymers 2024, 16, 2352. DOI https://doi.org/10.3390/polym16162352
- Mirek A., Grzeczkowicz M., Lamboux C., Syreina Sayegh S., Bechelany M., Lewińska D. “Formation of disaggregated polymer microspheres by a novel method combining pulsed voltage electrospray and wet phase inversion techniques.” Colloids and Surfaces A: Physicochemical and Engineering Aspects, Vol. 648, (2022), 129246, DOI: https://doi.org/10.1016/j.colsurfa.2022.129246
- Rosiński S., Lewińska D., Migaj M., Woźniewicz B., Weryński A. “Electrostatic microencapsulation of parathyroid cells as a tool for the investigation of cells activity after transplantation”; Landbauforschung Voelkenrode, Special Issue, 241, 47-50, 2002
- Lewińska D., Bukowski J., Kożuchowski M., Kinasiewicz A., Weryński A. “Electrostatic microencapsulation of living cells”. Biocyb and Biomed Eng, vol. 28(2), 69-84, 2008
- Jasińska U., Skąpska S., Owczarek L., Dekowska A., Lewińska D. „Immobilization of Bifidobacterium infantis cells in selected hydrogels as a method of increasing their survival in fermented milkless beverages” Journal of Food Quality, vol. 2018, doi.org/10.1155/2018/9267038
- Cendrowski P., Kramek-Romanowska K., Lewińska D., Grzeczkowicz M., Korycka P., Krzysztoforski J. “CFD modeling of droplet generation process for medical applications using the electrostatic impulse method” Chemical and Process Engineering 2022, 43 (3), 331–355., DOI: 10.24425/cpe.2022.142278
- Lewińska D., Chwojnowski A., Wojciechowski C., Kupikowska-Stobba B., Grzeczkowicz M., Weryński A. „Electrostatic droplet generator with 3-coaxial-nozzle head for microencapsulation of living cells in hydrogel covered by synthetic polymer membranes” Sep Sci and Technol, vol. 47(3), 463-469, 2012
- Lewińska D., Grzeczkowicz M., Kupikowska-Stobba B. “Influence of electric parameters on the alginate-polyethersulfone microcapsule structure” Desalination and Water Treatment vol. 64, 400-408, 2017 DOI: 10.5004/dwt.2017.11407. 64 (2017)
- Przytulska M., Kulikowski J. L., Lewińska D., Grzeczkowicz M., Kupikowska-Stobba B. „Computer-Aided Image Analysis for Microcapsules’ Quality Assessment.” Biocybernetics and Biomedical Engineering, vol. 35(4):342-350, 2015, DOI:10.1016/j.bbe.2015.05.005
- Mirek A., Korycka P., Grzeczkowicz M. Lewińska D.,(2019) “Polymer fibers electrospun using pulsed voltage” Materials and Design 183 (2019) 108106, DOI: 10.1016/j.matdes.2019.108106
- Mirek A., Grzeczkowicz M., Belaid H., Bartkowiak A., Barranger F., Abid M., Wasyłeczko M., Pogorielov M., Bechelany M., Lewińska D., “Electrospun UV-cross-linked polyvinylpyrrolidone fibers modified with polycaprolactone/polyethersulfone microspheres for drug delivery” Biomaterials Advances 147 (2023) 213330, https://doi.org/10.1016/j.bioadv.2023.213330
- Kupikowska-Stobba B., Grzeczkowicz M., Lewińska D., “A one-step in vitro continuous flow assessment of protein release from core-shell polymer, microcapsules designed for therapeutic protein delivery.” Biocybernetics and Biomedical Engineering, vol. 41 (2021) 1347– 1364, 2021, DOI https://doi.org/10.1016/j.bbe.2021.05.003
- Kupikowska-Stobba B., Lewińska D., “Polymer microcapsules and microbeads as cell carriers for in vivo biomedical applications”, Biomaterials Science, 2020, DOI: 10.1039/c9bm01337g
- Lewińska D., Rosiński S., Hunkeler D., Poncelet D., Weryński A. “Mass transfer coefficient in characterization of gel beads and microcapsules” J. Membrane Sci, vol. 209(2): 533-540, 2002
- Hunkeler D., Wandrey Ch., Rosiński S., Lewińska D., Weryński A. Characterization of microcapsules (in: Fundamentals of Cell Immobilisation Biotechnology, eds. Nedovič V, Willaert R), Kluwer Academic Publishers, Dordrecht, Boston, London, 8A, 389-410, 2004
- Grzeczkowicz M., Lewińska D. “A method for investigating transport properties of partly biodegradable spherical membranes using vitamin B12 as marker” Desalination and Water Treatment, 128:170-178, 2018 , doi: 10.5004/dwt.2018.22631
- Kupikowska-Stobba B., Lewińska D., Grzeczkowicz M. „Chemical method for retrieval of cells encapsulated in alginate-polyethersulfone microcapsules”, Artificial Cells, Nanomedicine, and Biotechnology vol. 42(3): 151-160, 2014 DOI:10.3109/21691401.2013.800083
- Lewińska D., Rosiński S., Weryński A. “Influence of process conditions during impulsed electrostatic droplet formation on size distribution of hydrogel beads” Artif Cell, Blood Substitutes and Biotechnol, vol. 32, 1, 41-53, 2002
- Prusse U., Bilancetti L., Bucko M., Bugarski B., Bukowski B., Gemainer P., Lewińska D., Massart B., Nastruzzi C., Nedovic V., Poncelet D., Siebenhaar S., Tobler L., Tosi A., Vikartovska A., Vorlop K-D. “Comparison of different technologies for alginate bead production”. Chem Papers, vol. 62(4), 364-374, 2008
- Kupikowska B., Lewińska D., Dudziński K., Jankowska-Śliwińska J., Grzeczkowicz M., Wojciechowski C. “The influence of changes in composition of membrane-forming solution on the structure of alginate-polyethersulfone microcapsules”. Biocyb and Biomed Eng, vol. 29(3), 61-69, 2009
- Mirek A., Belaid H., Barranger F., Grzeczkowicz M., Bouden Y., Cavaillès V., Lewińska D, Bechelany M., “Development of a new 3D bioprinted antibiotic delivery system based on a cross-linked gelatin–alginate hydrogel.” J. Mater. Chem. B, 2022, Advance Article, DOI https://doi.org/10.1039/D2TB01268E
- Mirek A., Belaid H., Bartkowiak A., Barranger F., Salmeron F., Kajdan M, Grzeczkowicz M., Cavaill`es V., Lewinska D., Bechelany M. „Gelatin methacrylate hydrogel with drug-loaded polymer microspheres as a new bioink for 3D bioprinting.”, Biomaterials Advances 150 (2023) 213436, DOI: https://doi.org/10.1016/j.bioadv.2023.213436
Patenty:
- Korycka P., Mirek A., Lewińska D., Grzeczkowicz M., Chwojnowski A: “Sposób wytwarzania biodewgradowalnej membrany polimerowej.” PATENT RP Nr 237648, 2021 r.
- Lewińska D., Kupikowska-Stobba B., Grzeczkowicz M., Chwojnowski A., Łukowska E.: „Sposób oznaczania stężenia komórek.” PATENT RP Nr 223717, 2012
- Lewińska D., Chwojnowski A., Jankowska-Śliwińska J., Weryński A.: „Mikrokapsułki zawierające substancje biologicznie aktywne, zwłaszcza żywe komórki i/lub mikroorganizmy, ewentualnie genetycznie modyfikowane, albo naturalne lub syntetyczne do zastosowań biomedycznych, sposób ich wytwarzania oraz urządzenie do stosowania tego sposobu”, . PATENT RP Nr 208383, 2007
- Lewińska D., Bukowski J., Rosiński S,. Kożuchowski M., Weryński A.: ”Sposób jednoetapowego wytwarzania mikrokapsułek, zwłaszcza zawierających żywe komórki, ich zbiory lub substancje biologicznie aktywne, oraz urządzenie do ich wytwarzania”, PATENT RP Nr 208384, 2004
Współpraca międzynarodowa:
- W latach 2020-2024 współpraca z Universite de Montpellier we Francji w ramach umowy pt.:”International Join Doctorate Convention” zawartej pomiedzy w/w instytutem a IBIB PAN w dniu 30.04.2020 r. dotycząca współprowadzenia przewodu doktorskiego mgr inż. Adama Mirka
- W latach 2005-2007 w ramach dwustronnego projektu Polonium współpraca z grupą prof. Cecile Legallais z University of Technology, Compiegne, CNRS, UMR 6600, Compiegne Francja w temacie: „Modification of alginate beads with hepatocytes for bioartificial liver.”
- W latach 1999-2004 w ramach Europejskiego Projektu Akcja COST 840 “Bioencapsulation. Innovations and Technologies.” bezpośrednia współpraca z naukowcami z następujących jednostek naukowo-badawczych:
- Institute of Technology and Biosystems Engineering Federal Agricultural Research Centre (FAL) obecnie: Thüne Insitute of Agricultural Technology, Brunszwik, Niemcy;
- Institute of Chemistry Slovak Academy of Sciences, Bratysława, Słowacja;
- Depqtartment of Chemical Engineering Faculty of Technology and Metallurgy, Belgrad Serbia i Czarnogóra;
- ENITIAA, UMR CNRS GEPEA, Nantes, Francja;
- Laboratory of Polyelectrolytes and Biomacromolecules, Swiss Federal Institute of Technology, Lozanna, Szwajcaria;
- Institute of Pharmaceutical Technology and Biopharmaceutics, University of Vienna, Austria;
School of Chemical Engineering, University of Birmingham, Edgbaston, Birmingham, Wielka Brytania; - Laboratory of Chemical and Biological Engineering, Swiss Federal Institute of Technology, Lozanna, Szwajcaria;
- Departament of Pharmacy and Pharmaceutical Technology, University of Basque Country, Vitoria, Hiszpania.
Granty:
- Projekt badawczy Nr N N518 415136 pt.: ”Opracowanie sposobu wytwarzania jednorodnych membran polimerowych w nowych mikrokapsułkach alginianowo-polieterosulfonowych z wykorzystaniem metod i algorytmów komputerowej analizy obrazów.” 2009-2011.
- Specjalna dotacja KBN SPUB-M Nr 56/E-83/ SPUB/COST/P-04/DZ584/2002-2003 pt.: „Opracowanie i zbadanie zmodyfikowanego elektrostatycznego generatora mikrokapsułek. Wykonanie badań transportowych mikrokapsułek wytwarzanych w ramach projektu COST 840” 2002-2004.
Projekt badawczy PB 538/PO5/98/15 pt.: ”Nowa strategia terapeutyczna w transplantologii. Allotransplantacja komórek przytarczyc ludzkich in vitro w leczeniu niedoczynności przytarczyc bez immunosupresji”1998-2001
- Specjalna dotacja KBN SPUB-M Nr 56/E-83/ SPUB/COST/P-04/DZ 62/99 pt.: „Akcja COST 840 – Dobór warunków procesu wywarzania mikrokapsułek przy pomocy pola elektrostatycznego oraz opłaszczania mikrokapsułek membraną i opracowanie metody badania ich własności transportowych in vitro”1998-2001.
2. Opracowywanie nowych, polimerowych rusztowań komórkowych do regeneracji chrząstki stawowej.
Drugi temat badawczy prowadzony w Pracowni EMB, kierowany przez prof. Andrzeja Chwojnowskiego dotyczy opracowywana nowych, polimerowych rusztowań komórkowych do regeneracji chrząstki stawowej. Dlaczego to robimy?
Dlaczego to robimy?
Z każdym rokiem liczba pacjentów cierpiących na uszkodzenia chrząstki stawowej rośnie. Urazy te znacząco obniżają komfort życia chorych. Niestety, obecnie nie istnieje w pełni skuteczna metoda regeneracji chrząstki. Jednym z najbardziej obiecujących podejść jest zastosowanie rusztowań komórkowych, które stanowią podporę dla komórek chrząstki (chondrocytów) lub komórek macierzystych, wspomagając ich rozwój oraz regenerację.
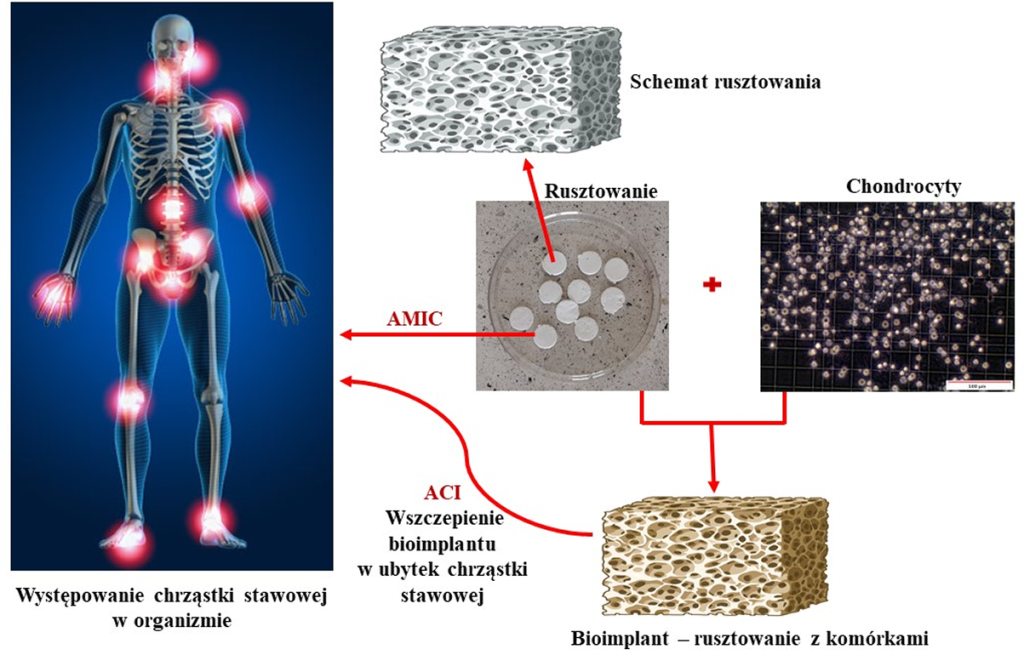
Rys. 10. Występowanie chrząstki stawowej w ogranizmie oraz schemat metod terapeutycznych z wykorzystaniem rusztowań komórkowych do regeneracji chrząstki stawowej.
Jak pracujemy?
W naszym laboratorium specjalizujemy się w projektowaniu i otrzymywaniu rusztowań komórkowych, które mogą znaleźć zastosowanie w najbardziej obiecujących metodach terapeutycznych, takich jak ACI (autologiczny przeszczep chondrocytów, ang. Autologous Chondrocyte Implantation) i AMIC (autologiczna chondrogeneza indukowanamacierzą, ang. Autologous Matrix-Induced Chondrogenesis). Opracowujemy rusztowania o kontrolowanej porowatości, bioaktywności i biodegradacji, aby jak najlepiej wspierały regenerację chrząstki stawowej [1].
Każde opracowane rusztowanie przechodzi badania obejmujące:
- Analizę struktury – obrazowanie za pomocą skaningowego mikroskopu elektronowego (SEM) oraz zaawansowanego oprogramowywania MeMoExplorer, które umożliwia dokładną analizę i ocenę geometrii porów i ich rozmieszczenie, a także otrzymanie wyników, z którym można uzyskać dane odnośnie powtarzalności struktur rusztowań [2]. W badaniach koncentrujemy się na otrzymywaniu rusztowań, które umożliwiają hodowlę komórek macierzystych i chondrocytów, dostosowaną do ich specyficznych wymaga. Odpowiednia wielkość porów jest niezbędna do otrzymania rusztowań, które mogą znaleźć zastosowanie w skutecznej terapii dostępnymi metodami ACI i AMIC. Aby zapewnić optymalne warunki do wzrostu i różnicowania komórek, projektujemy rusztowania z odpowiednią wielkością porów. Dla komórek macierzystych rusztowania o porach powyżej 300 µm, natomiast chondrocyty wymagają mniejszych porów, poniżej 300 µm.
Otrzymywane rusztowania, mimo wykorzystywania różnych polimerów, charakteryzują się powtarzalnością oraz zróżnicowaną wielkością porów [3-6].
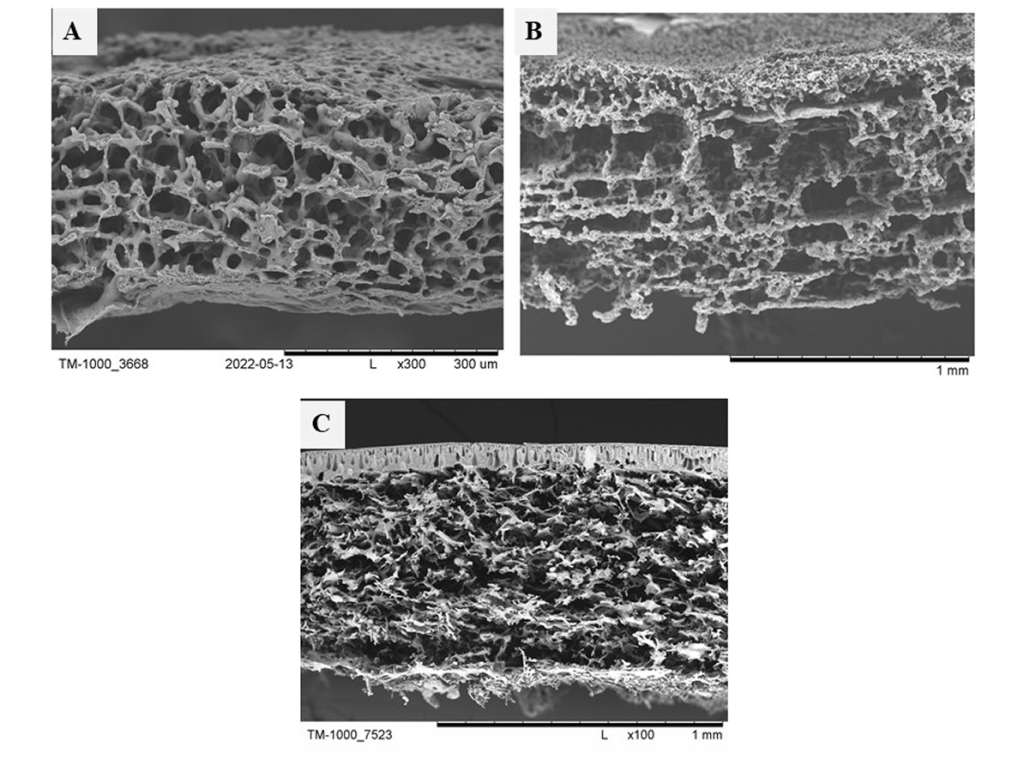
Rys. 11. Obrazy SEM rusztowań zaprojektowanych i otrzymanych w Laboratorium Membran Półprzepuszczalnych. Rusztowanie zostały otrzymane z: A – mieszaniny polimerów PES i PUR; B – kopolimeru polilaktyd-ko-kaprolakton; C – z polieterosulfonu [3-6].
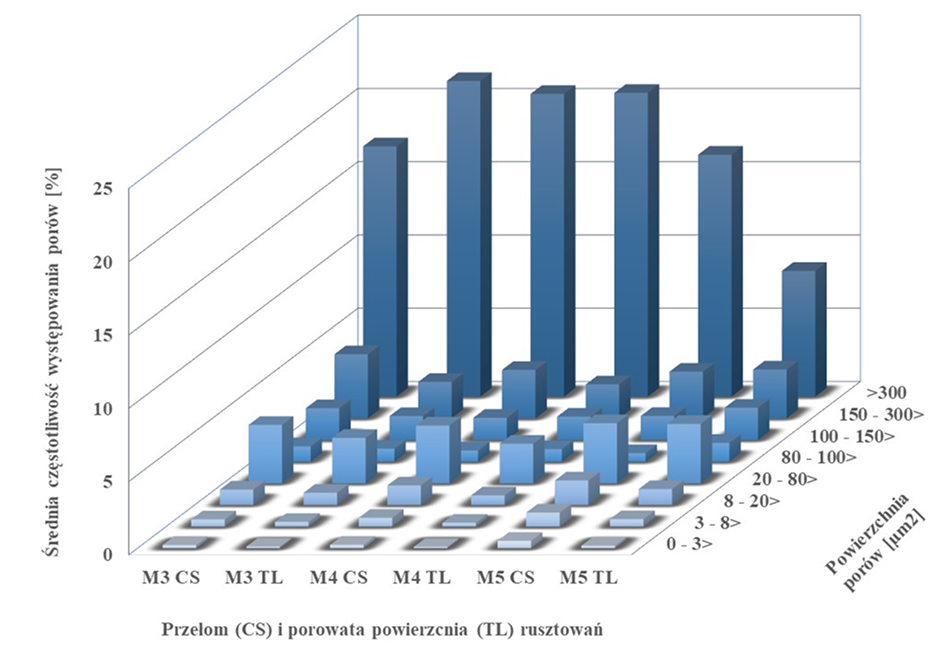
Rys. 12. Diagram przedstawia średnią częstotliwość występowania porów w ośmiu klasach
wielkości porów w przełomie rusztowań (CS) oraz na powierzchni rusztowań (TL). Diagram został
wykonany na podstawie oprogramowania MeMo Explorer [3].
- Właściwości mechaniczne – kluczowe dla biomechaniki stawu, w tym wytrzymałość i elastyczność [3];
- Porowatość i zwilżalność – niezbędne do zasiedlania komórek i transportu składników odżywczych [3];
- Bioegradacja – z wykorzystaniem płynów fizjologicznych, na przykład W symulowanym płynie fizjologicznym (SBF, ang Simulated Body Fluid) [3], [4].
Badania In Vitro i In Vivo
Najbardziej obiecujące rusztowania były poddawane dalszej walidacji:
- In vitro – testy z wykorzystaniem izolowanych chondrocytów ludzkich, pozwalające ocenić zdolność rusztowania do wspierania proliferacji i różnicowania komórek [6].
- In vivo – wybrane rusztowania poddano badaniom na modelu królika, które przeprowadzono we współpracy z lekarzami ortopedami ze Szpitala Uniwersyteckiego Ortopedyczno-Traumatologicznego Gruca, Oddział Traumatologii i Ortopedii w Otwocku [7-9].
Jeśli chcesz dowiedzieć się więcej o naszych badaniach i rusztowaniach lub nawiązać współpracę, zapraszamy do kontaktu!
Wybrane publikacje:
- M. Wasyłeczko, W. Sikorska, A. Chwojnowski, Review of synthetic and hybrid scaffolds in cartilage tissue engineering, Membranes. 10 (2020) 1–28. https://doi.org/10.3390/membranes10110348.
- M. Przytulska, J.L. Kulikowski, M. Wasyłeczko, A. Chwojnowski, D. Piętka, The evaluation of 3D morphological structure of porous membranes based on a computer-aided analysis of their 2D images, Desalination and Water Treatment. 128 (2018). https://doi.org/10.5004/dwt.2018.22569.
- M. Wasyłeczko, E. Remiszewska, W. Sikorska, J. Dulnik, A. Chwojnowskl, Scaffolds for Cartilage Tissue Engineering from a Blend of Polyethersulfone and Polyurethane Polymers, Molecules (Basel, Switzerland). (2023) 1–25. https://doi.org/10.3390/molecules28073195.
- M. Wasyłeczko, W. Sikorska, M. Przytulska, J. Dulnik, A. Chwojnowski, Polyester membranes as 3D scaffolds for cell culture, Desalination and Water Treatment. 214 (2021) 181–193. https://doi.org/10.5004/dwt.2021.26658.
- K. Dudziński, A. Chwojnowski, M. Gutowska, M. Płończak, J. Czubak, E. Łukowska, C. Wojciechowski, Three dimensional polyethersulphone scaffold for chondrocytes cultivation – The future supportive material for articular cartilage regeneration, Biocybernetics and Biomedical Engineering. 30 (2010) 65–76.
- M. Wasyłeczko, Z.J. Krysiak, E. Łukowska, M. Gruba, W. Sikorska, A. Kruk, J. Dulnik, J. Czubak, A. Chwojnowski, Three-dimensional scaffolds for bioengineering of cartilage tissue, Biocybernetics and Biomedical Engineering. 42 (2022) 494–511. https://doi.org/10.1016/j.bbe.2022.03.004.
- M. Baranowski, M. Wasyłeczko, A. Kosowska, A. Plichta, S. Kowalczyk, A. Chwojnowski, W. Bielecki, J. Czubak, Regeneration of Articular Cartilage Using Membranes of Polyester Scaffolds in a Rabbit Model, Pharmaceutics. 14 (2022). https://doi.org/10.3390/pharmaceutics14051016.
- M. Płończak, M. Wasyłeczko, T. Jakutowicz, A. Chwojnowski, Intraarticular Implantation of Autologous Chondrocytes Placed on Collagen or Polyethersulfone Scaffolds : An Experimental Study in Rabbits, (2023) 4–7.
- T. Jakutowicz, M. Wasyłeczko, M. Płończak, C. Wojciechowski, A. Chwojnowski, J. Czubak, Comparative Study of Autogenic and Allogenic Chondrocyte Transplants on Polyethersulfone Scaffolds for Cartilage Regeneration, 2024. https://doi.org/10.3390/
Patenty:
- A. Chwojnowski, E, Łukowska, C. Wojciechowski, M. Wasyłeczko, W. Sikorska, Z. Krysiak, „Sposób wyodrębniania białka z hodowli komórkowych prowadzonych na rusztowaniach komórkowych”. PATENT PL 238140, 2021
- A. Chwojnowski, E. Łukowska, C. Wojciechowski, M. Wasyłeczko, W. Sikorska, Z. Krysiak, „Sposób wykrywania pozostałości celulozy w półprzepuszczalnych membranach szeroko porowatych”. PATENT PL 235794, 2020
- E. Łukowska, A. Szakiel, M. Markowski, M. Wasyłeczko, A. Chwojnowski, S. Martyniuk, „Wielowarstwowa membrana poliestrowa i sposób jej wytwarzania.” PL 239461, 2019
3. Półprzepuszczalne, kapilarne membrany polimerowe o różnych właściwościach
W ramach trzeciego kierunku badawczego opracowywane, wytwarzane i badane są półprzepuszczalne, kapilarne membrany polimerowe o różnych właściwościach, dostrajanych do specyficznych potrzeb w zastosowaniach biomedycznych (np. hodowle komórkowe) i biotechnologicznych (np. membrany „antyfoulingowe”).
Membrany otrzymywane są metodą przędzenia na opracowanej przez Zespół instalacji do otrzymywania membran kapilarnych metodą mokrej inwersji faz poprzez wytłoczenie roztworu polimeru przez filierę formułującą kapilarę. Wytwarzamy membrany z polisulfonu (PSf), polieterosulfonu (PES), octanu celulozy (OC), poliuretanu (PU) oraz mieszane. Poprzez zmiany parametrów przędzenia membran mamy możliwość otrzymywania membran o pożądanych parametrach transportowo-separacyjnych [1].


Opracowano także metodę wytwarzania membran dwuwarstwowych np. PSf/PU, PSf/OC, otrzymywanych za pomocą specjalnej filiery, w których jeden polimer tworzy warstwę zewnętrzną, a drugi wewnętrzną i polimery te nie mieszającą się ze sobą.
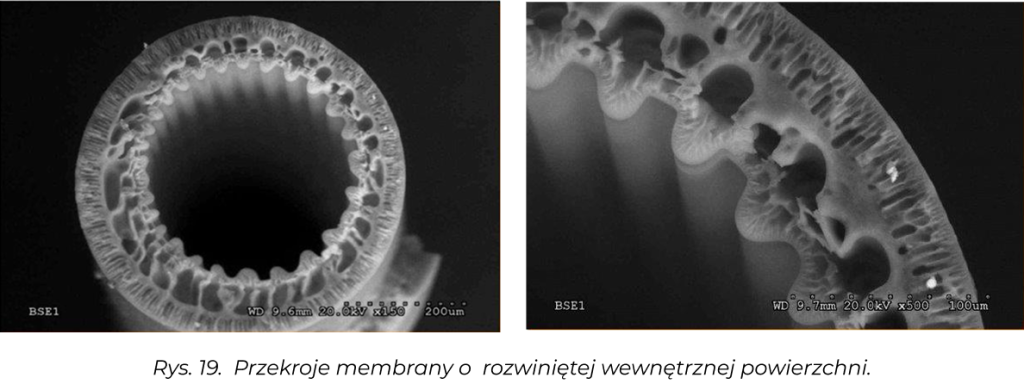
Degradowalne membrany wieloskładnikowe zbudowane są z polimeru bazowego stanowiącego trwałą konstrukcje membrany i polimeru degradowalnego, usuwanego ze struktury membran w czasie ich pracy. Mimo zachodzącego foulingu (zatykania porów membrany przez separowane bądź oczyszczane substancje) usuwany stopniowo polimer zwiększa porowatość membrany, co wydłuża czas jej pracy. Polimerem bazowym jest najczęściej PSf lub PES, polimerami degradowalnymi są: OC [3], polilaktyd, polikaprolakton, poliglikolid, kopolimer laktyd-glikolit-kaprolakton) [4] oraz PU [5-8].
Badane są właściwości transportowo-separacyjne membran takie jak przepuszczalność hydrauliczna (współczynnik ultrafiltracji UFC), retencje (wyznaczanie punktu odcięcia) oraz porowatość struktury membran określana za pomocą analizy zdjęć SEM [9-11], przeprowadzonej z użyciem opracowanego w naszym Instytucie programu komputerowego MeMoExplorerTM [12].
Współpracujemy z innymi pracowniami naszego Instytutu opracowując i wykonując dla nich membrany i mini-moduły membranowe stosowane w bioreaktorach [13-15] i hodowlach komórkowych.
Istotną działalnością naszej pracowni jest dydaktyka. Studenci Politechniki Warszawskiej realizują u nas prace inżynierskie, magisterskie i doktorskie. Prowadzone są ćwiczenia i praktyki studenckie.
Wybrane publikacje:
- C. Wojciechowski, A. Chwojnowski, K. Dudzinski, E. Lukowska. Evaluation of separation characteristic of polysulfone membranes modified by polymer solvents etching. Desalination and Water Treatment, vol 35, 263-270, 2011.
- A. Chwojnowski, C. Wojciechowski, K. Dudziński, E. Łukowska. Polysulphone and polyethersulphone hollow fiber membranes with developed inner surface as material for bio-medical applications. Biocybernetics and Biomedical Engineering. Vol. 29, No. 3, 47-59, 2009
- C. Wojciechowski, A. Chwojnowski, L. Granicka, E. Łukowska. Polysulfone/cellulose acetate blend semi degradable capillary membranes preparation and characterization. Desalination and Water Treatment. vol 64, 365-371, 2017
- C. Wojciechowski, M. Mazurek-Budzyńska, A. Palinska, A. Chwojnowski, L.Granicka, W. Sikorska, G. Rokicki. Preparation and characterization of partially degradable hollow fiber membranes based on polysulfone/poly(L-lactide-co-glycolide-co-ε-caprolactone) blends. Desalination and Water Treatment. vol 202, 38-47, 2020
- C. Wojciechowski, A. Chwojnowski, L. Granicka, E. Łukowska, M. Grzeczkowicz. Polysulfone/polyurethane blend degradable hollow fiber membranes preparation and transport-separation properties evaluation. Desalination and Water Treatment. vol 57, 22191-22199, 2016
- W. Sikorska, C. Wojciechowski, M. Przytulska, G. Rokicki, M. Wasyłeczko, J. Kulikowski, A. Chwojnowski. Polysulfone–polyurethane (PSf-PUR) blend partly degradable hollow fiber membranes: preparation, characterization, and computer image analysis. Desalination and Water Treatment. vol 128, 383-391, October 2018
- W. Sikorska, M. Wasyłeczko, M. Przytulska, C. Wojciechowski, G. Rokicki, A. Chwojnowski. Chemical Degradation of PSF‐PUR Blend Hollow Fiber Membranes—Assessment of Changes in Properties and Morphology after Hydrolysis. Membranes.vol. 11, 51, 12 January 2021
- W. Sikorska, M. Milner-Krawczyk , M. Wasyłeczko, C. Wojciechowski, A. Chwojnowski. Biodegradation Process of PSF-PUR Blend Hollow Fiber Membranes Using Escherichia coli Bacteria—Evaluation of Changes in Properties and Porosity. Polymers. 13, 1311, 16 April 2021
- A. Chwojnowski, C. Wojciechowski, D. Lewińska, E. Łukowska, J. Nowak, B. Kupikowska- Stobba, M. Grzeczkowicz. Studies on the structure of semi-permeable membranes by means of SEM. Problems and potential sources of errors. Biocybernetics and Biomedical Engineering, vol 32, numb.1, 51-64, 2012.
- A. Chwojnowski, M. Przytulska, D. Wierzbicka, J. Kulikowski, C. Wojciechowski. Membranes’ porosity evaluation by komputer-aided analysis of SEM images – A preliminary study. Biocybernetics and Biomedical Engineering. vol 32, numb.4, 65-75, 2012
- M. Przytulska, A. Kruk, J. Kulikowski, C. Wojciechowski, A. Gadomska-Gajadhur, A. Chwojnowski. Comparative Assessment of Polyvinylpirrolidone. Type of membranes. Based on porosity analysis. Desalination and Water Treatment. vol 75, 18–25, May 2017
- Sikorska W., Przytulska M., Wasyłeczko M., Wojciechowski C., Kulikowski J.L., Chwojnowski A. Influence of hydrolysis, solvent and PVP addition on the porosity of PSF/PUR blend partly degradable hollow fiber membranes evaluated using the MeMoExplorer software. Desalination and Water Treatment. 214, 114–119, February 2021
- A. Ciechanowska, P. Ładyżyński, G. Hoser, S. Sabalińska, J. Kawiak, P. Foltyński, C. Wojciechowski, A. Chwojnowski. Human endothelial cells hollow fiber membrane bioreaktor as a model of the blood vessel for in vitro studies. Journal of Artificial Organs. vol. 19, Issue 3, pp 270–277, Sept. 2016
- 1K. Pluta, M. Jakubowska; M. Wisniewska; A. Wencel; C. Wojciechowski; M. Gora; K. Dudek; A. Chwojnowski; B. Burzynska; D. Pijanowska. Hollow Fiber Bioreactor with Genetically Modified Hepatic Cells as a Model of Biologically Active Function Block of the Bioartificial Liver. Biocybernetics and Biomedical Engineering. Vol. 44(1), 9-19, 2023(4)
- P. Ładyżynski, A. Ciechanowska, S. Sabalinska, P. Foltynski, A. Wencel, C. Wojciechowski, K. Pluta, A. Chwojnowski. Development of an Artificial Blood Vessel Model in a Capillary Bioreactor and Assessment of the Effect of Glucose Levels on HUVECs Under Physiological Shear Stress, Biocybernetics and Biomedical Engineering. 44, 543–559, 2024